异基因造血干细胞移植治疗骨髓纤维化研究进展
原发性骨髓纤维化(MF)是一种克隆性骨髓增殖性疾病,主要见于中老年人。其特点为骨髓纤维化,脾脏肿大,外周血出现幼稚红细胞、幼稚粒细胞。而其他骨髓增殖性疾病如真性红细胞增多症(PV)或原发性血小板增多症(ET)并发的骨髓纤维化,称为Post-PV/ET MF。异基因造血干细胞移植(allo-HSCT)是目前唯一可能治愈MF的方法。本文就MF患者的移植适应证、影响移植疗效的因素、移植后微小残留病(MRD)监测和复发的治疗等研究进展进行如下综述。
一、移植适应证
MF患者的预后差异极大,确诊后应根据国际预后积分系统(IPSS)、动态国际预后积分系统(DIPSS)及DIPSS-plus(表1)进行预后分组。IPSS分组:低危(0分)、中危-1(1分)、中危-2(2分)、高危(≥3分);DIPSS分组:低危(0分)、中危-1(1或2分)、中危-2(3或4分)、高危(5或6分);DIPSS-plus分组:低危(0分)、中危-1(1分)、中危-2(2或3分)、高危(4~6分)。
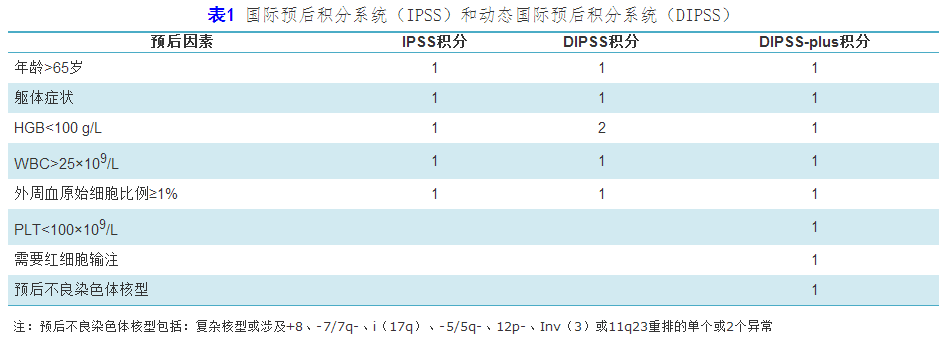
目前研究证实,按IPSS、DIPSS、DIPSS-plus分期为中危-2及高危组的MF患者,中位总生存(OS)时间<5年,如有合适供者,应尽早行allo-HSCT。Kröger等比较了438例原发性MF患者接受allo-HSCT或传统治疗的疗效差异,结果显示,DIPSS低危组患者接受两种方式治疗后5年OS率分别为69%、95%,中危-1组分别为52%、77%,中危-2组分别为50%、41%,高危组分别为32%、11%。与传统治疗相比,低危组患者allo-HSCT的死亡相对危险度(RR)为5.6,而中危-1组为1.6,中危-2组为0.55,高危组为0.37。
由此可以看出,低危组患者明显获益于传统治疗,而中危-2组、高危组患者明显获益于allo-HSCT。因此,低危组患者应首选传统治疗,中危-2及高危组患者应首选allo-HSCT。而对于中危-1组患者,欧洲骨髓移植组织(EBMT)/欧洲白血病网(ELN)工作组建议:如果该组患者伴有以下危险因素:输血依赖、外周血原始细胞>2%或具有DIPSS-plus评分系统中的不良染色体核型,如有合适供者,也应行allo-HSCT治疗。此外,有研究证实伴有ASXL1突变或JAK2、CALR、MPL突变阴性的MF患者,病程进展快,生存期短,因此,EBMT/ELN工作组建议这类患者也宜尽早行allo-HSCT。
二、影响患者移植疗效的因素
(一)患者因素
1.年龄
近年来,由于减剂量预处理(RIC)方案的应用、支持治疗的改善,越来越多的老年患者也适合行allo-HSCT。Samuelson等对30例年龄60~78岁MF患者行allo-HSCT,移植后3年OS、无进展生存(PFS)率分别可达45%、40%。Gupta等回顾性分析了233例MF患者allo-HSCT后疗效,结果显示年龄>60岁者与41~60岁者比较,OS和PFS率差异均无统计学意义。此外,Rondelli等在MPD-RC 101前瞻性研究中也发现MF患者移植后的OS率与年龄无关。所以,高龄不是MF患者行allo-HSCT的绝对禁忌证。
2.危险度分层
MF患者的危险度分层与allo-HSCT疗效明显相关,危险度越低,疗效越好。Scott等[8]报道了170例MF患者allo-HSCT疗效,DIPSS低危、中危-1、中危-2和高危组患者移植后6年OS率分别为80%、67%、54%、38%。与低危组患者相比,高危组患者移植后死亡和非复发死亡(NRM)的危险度(HR)分别为4.11、3.41。同样,Ditschkowski等的研究也支持这一观点。该研究中,DIPSS低危组患者移植后5年OS率明显高于中危-1、中危-2/高危组患者。因此,MF患者在疾病早期allo-HSCT疗效较好。
3.共患病
与其他疾病一样,MF患者的共患病对allo-HSCT疗效也有影响。Scott等发现共患病指数(HCT-CI)高的患者移植后总病死率、NRM率均较高。此外,Kerbauy等对行allo-HSCT的104例MF患者研究发现,HCT-CI是影响患者移植后OS的独立预后因素。Ditschkowski等研究也得出类似结论。因此,患者的共患病也是影响allo-HSCT疗效的重要因素,HCT-CI高的患者疗效较差。
4.基因突变
JAK2、CALR和MPL突变是MF的三个特征性基因突变,不少研究证实伴有这类基因突变的患者allo-HSCT疗效往往较好。Kröger等[11]研究了103例MF患者的allo-HSCT疗效,其中59例伴有JAK2 V617F突变,结果发现JAK2突变组患者移植后3年无病生存(DFS)率、5年OS率均较高。同样,Alchalby等先后分析了139例、150例MF患者资料,也发现伴有JAK2 V617F突变的患者移植后OS率较高。因此,具有JAK2突变的MF患者allo-HSCT预后较好。此外,Panagiota等分析了133例MF患者allo-HSCT疗效,发现伴有CALR突变者移植后4年OS率较无CALR突变者高;进一步分析还发现伴有CALR突变的患者预后最好,伴MPL或JAK2突变者次之,而不伴有这三种突变者预后最差。因此,CALR突变也是allo-HSCT预后良好的标志。
5.MF严重程度
目前研究证实MF严重程度与患者allo-HSCT疗效明显相关,MF越严重,疗效越差。Alchalby等采用allo-HSCT治疗97例MF-3级患者和50例MF≤2级患者,结果发现MF-3级患者移植后OS较差。Kerbauy等的研究也证实这一观点。此外,Kröger等发现allo-HSCT后纤维化恢复程度对移植预后也有明显影响。该研究分析了57例MF患者的移植疗效,其中41例患者MF-3级,结果发现95%患者移植物成功植活,且移植后100 d MF≤1级的患者5年OS率明显高于MF>1级者。由此可见,MF严重程度是影响allo-HSCT疗效的重要因素,且allo-HSCT后纤维化迅速恢复者可能预后较好。
(二)供者因素
1.供者来源
MF患者行allo-HSCT应首选HLA匹配同胞供者(MSD)移植。Gupta等[6]对233例原发性MF患者资料进行分析,其中MSD移植79例,HLA匹配无关供者(MUD)移植104例,HLA部分匹配/不匹配无关供者移植50例,结果发现MSD移植患者5年OS率较高,NRM较低。此外,Rondelli等在MPD-RC 101前瞻性研究中比较了32例MSD移植和34例MUD移植的疗效差异,发现前者植入失败率较低,OS率较高。Robin等的研究也得出类似结论。可以看出,MSD移植可以减少植入失败发生,改善移植预后。因此MSD是最佳供者来源。
对于缺乏MSD的MF患者,MUD或半倍体移植是有效的治疗选择。多项研究发现MSD和MUD移植疗效相当。Ballen等报道了289例MF患者的移植结果,其中162例患者接受MSD移植,101例接受MUD移植,余26例接受HLA不匹配的亲缘供者移植,结果显示三组患者移植后5年OS率差异无统计学意义。此外,Bregante等分析了95例MF患者资料,发现MUD和半倍体移植疗效在近些年明显改善。该研究中,2011年至2014年接受MUD移植或半倍体移植患者的OS率高于2000年至2010年接受同种治疗的患者。因此,对于缺乏MSD的患者,也可采用MUD或半倍体移植替代治疗。
2.造血干细胞来源
多项研究发现外周血干细胞移植(PBSCT)比骨髓移植(BMT)更有利于植入,因此,EBMT/ELN工作组建议MF患者首选PBSCT。Kerbauy等比较了104例MF患者PBSCT或BMT的疗效差异,发现PBSCT组患者植入快,中性粒细胞植入时间早于BMT组患者5.7 d。Anasetti等分析了273例PBSCT和278例BMT患者资料,发现两组患者移植后OS率相当,但PBSCT组患者移植失败率明显较低。因此,MF患者应首选allo-PBSCT。
脐血移植(UCBT)存在植入延迟、植入失败率高等问题,其临床应用受到限制。Murata等发现UCBT组与MSD-BMT组患者相比,中性粒细胞植入率、血小板植入率均较低。Robin等对35例MF患者行UCBT,发现高达40%的患者发生植入失败。然而,该研究中采用TBI、氟达拉滨联合环磷酰胺(TCF)进行预处理的17例患者均重建造血,且RIC TCF预处理患者移植后无事件生存(EFS)率明显较高。因而该研究者认为以TCF为基础的RIC方案可能改善UBCT患者的预后,不过这还有待进一步证实。多数学者认为UCBT疗效较差,需更多的临床试验以积累经验。
(三)治疗相关因素
1.预处理方案
清髓性预处理(MAC)方案由于移植相关死亡率(TRM)高,主要适用于年轻及一般状况较好的MF患者。而对于老年患者和存在合并症的患者,适合选择RIC方案。众多研究比较了MAC和RIC方案疗效,发现两者疗效相当。Stewart等对51例MF患者进行allo-HSCT,发现MAC组患者复发率较RIC组低。Gupta等的研究也得出类似结论。此外,Olsson等发现MAC方案促进植入,减少移植失败。因此,年轻及一般状况较好的患者应首选MAC方案移植。
RIC allo-HSCT可以降低TRM,使越来越多的老年患者及存在合并症患者可以接受移植。RIC方案中氟达拉滨联合白消安(FB)/马法兰(FM)或TBI是最常用的方案。Kroger等[11]对103例MF患者进行RIC allo-HSCT,采用FB方案联合抗胸腺细胞球蛋白(ATG)预处理,结果取得较肯定的疗效,98%的患者成功植入,移植后1年NRM为16%,5年OS率为67%。杨隽等采用FB方案联合TBI作为RIC方案,成功治疗1例高危原发性MF患者。此外,Robin等比较了105例FB方案预处理和55例FM方案预处理的MF患者疗效,发现两组患者移植后7年OS率差异无统计学意义。综上,FB/FM方案预处理均可选择,但哪种方案更佳,还有待更多的前瞻性研究去证实。
2.移植前脾切除:
巨脾是影响MF患者allo-HSCT疗效的重要因素。Bacigalupo等[29]对46例原发性MF患者allo-HSCT疗效进行分析,发现脾脏>22 cm是影响移植预后的独立危险因素。移植前脾脏>22 cm的患者移植后OS率较低,TRM较高。关于移植前脾切除对移植疗效的影响尚存在争议。有研究者认为MF患者移植前进行脾切除可以提高allo-HSCT疗效。Robin等研究发现移植前脾切除的患者造血恢复快,植入率高,移植后OS率较高。然而,也有多项研究证实移植前行脾切除对移植后OS无明显影响。Akpek等分析了9683例骨髓增殖性肿瘤患者资料,其中472例患者移植前进行脾切除,300例患者移植前行脾区放疗,1 471例患者移植时伴有脾肿大,余7 440例患者移植时无脾肿大。研究发现,四组患者移植后3年OS率无显著差异。此外,尚有研究认为晚期MF患者脾切除反而影响allo-HSCT疗效。Santos等发现疾病进展期行脾切除的患者移植后5年OS率、无白血病生存(LFS)率均较差。可以看出,目前的研究不足以支持移植前脾切除,而且脾切除存在围手术期并发症和手术相关死亡的风险。基于这些考虑,移植前脾切除不作为常规推荐。
3.JAK抑制剂应用
关于移植前JAK抑制剂芦可替尼的应用,有研究发现移植前对芦可替尼治疗有效的MF患者allo-HSCT预后较好。Shanavas等研究了100例移植前接受芦可替尼治疗的MF患者的疗效,发现经芦可替尼治疗获得临床缓解的患者allo-HSCT后2年OS率明显高于治疗无效或疾病进展的患者。同样,Stübig等[33]也证实移植前对芦可替尼治疗有效的患者移植后OS率提高。因此,MF患者对芦可替尼治疗是否有效可能是影响allo-HSCT预后的重要因素。此外,有研究者认为移植前应用芦可替尼可减轻脾肿大,从而利于植入。Jaekel等对14例接受芦可替尼治疗的MF患者进行allo-HSCT,其中11例患者芦可替尼治疗前伴脾肿大(肋缘下7~25 cm),结果植入率高达93%。随访9个月,移植后OS、EFS率分别为78.6%、64%。关于移植前应用芦可替尼对移植预后的影响,由于数据较少,还有待更多大样本的研究结果予以证实。
(四)发生白血病转化
MF患者一旦发生急性白血病转化(LT),预后极差,中位生存期<5个月。2012年Tefferi等建立了一个积分系统用于评价发生LT的风险。该积分系统包括以下危险因素:不良染色体核型[单体核型,inv3或i(17q),积2分]、外周血原始细胞≥2%(积1分)、血小板减少(≤50×109/L,积1分)。积分为0、1、≥2分的患者,3年内LT的发生率分别为3%、10%、35%。因此,对于伴有以上任一危险因素的患者,建议在LT发生前接受allo-HSCT治疗。而对于已经发生LT的MF患者,allo-HSCT可使部分患者获得长生存。Alchalby等分析了46例LT患者的移植疗效,移植后3年OS、PFS率分别为33%、26%;移植前获得完全缓解(CR)的患者移植后OS明显较高。因此,EBMT/ELN工作组建议:LT患者移植前需行化疗,达CR或部分缓解后再行allo-HSCT。
三、移植后MRD监测和复发的治疗
如前所述,JAK2、MPL和CALR突变是MF的三个特征性基因突变,研究发现90%的MF患者至少携带其中一个突变。Kroger等发现实时定量PCR可以敏感地检测JAK2 V617F突变,利用这种技术检测JAK2突变进而可以监测MRD。Alchalby等分析了139例伴有JAK2 V617F突变的MF患者资料,发现移植后6个月外周血JAK2突变阴性预示复发率明显降低。Lange等发现移植后28 d JAK2 V617F等位基因负荷>1%的患者复发率较高。可以看出,对于伴有JAK2突变的MF患者,移植后监测JAK2水平可以有效预测复发。此外,也可利用CALR突变监测MRD,但目前的研究数据尚少。
对于移植后复发患者,如不伴有严重移植物抗宿主病(GVHD),免疫抑制剂减量或供者淋巴细胞输注(DLI)是目前有效的治疗手段。Kroger等对17例移植后复发MF患者行DLI治疗,其中临床复发9例,JAK2检测MRD阳性8例。结果发现,治疗后临床复发者的CR率为44%,GVHD发生率为18%;而分子水平复发者100%获得CR,无一例发生GVHD。可以看出,DLI治疗早期复发患者疗效更好,不良反应更小,也说明移植后进行分子水平监测的重要性。经上述治疗不能达CR的患者,可以考虑二次移植。
Klyuchnikov等对30例移植后复发或排斥的MF患者进行治疗,其中26例接受DLI治疗,对DLI治疗无效或不能耐受的17例患者行二次RIC allo-HSCT。随访27个月,30例患者的2年OS、PFS率分别达70%、67%。可以看出,DLI、二次移植是复发患者有效的挽救治疗方案。此外,对于移植后复发同时存在全身症状或脾肿大的患者,EBMT/ELN工作组建议可以联合应用JAK2抑制剂[3],但能否获益还有待更多研究结果证实。
综上,allo-HSCT是目前唯一可能治愈MF的手段。按IPSS、DIPSS、DIPSS-plus分期为中危-2组及高危组的患者,如有合适供者,应尽早行allo-HSCT。以MSD-PBSCT作为首选,MUD和半倍体移植也是有效的替代手段。最佳的预处理方案有待证实,但年轻及一般状况较好的MF患者应首选MAC方案,而老年及存在合并症患者适合RIC方案。移植前应用JAK2抑制剂可能对提高移植疗效有益,而移植前是否进行脾切除尚存在争议。此外,患者存在JAK2、CALR突变是移植预后良好标志,且这些标志可用于移植后分子水平监测,预示早期复发。而对于复发患者,及时给予DLI、二次移植等是有效的挽救治疗方案。








